
Зміст
Хоча всі атоми одного і того ж елемента містять однакову кількість протонів, кількість нейтронів може змінюватися. Знаючи, скільки нейтронів має певний атом, може допомогти вам визначити, чи є частинка правильною в цьому елементі, або ізотопом, який буде мати більш-менш нейтрони. Визначити кількість нейтронів в атомі досить просто і не вимагає експерименту. Щоб обчислити кількість нейтронів у звичайному атомі чи ізотопі, дотримуйтесь цих інструкцій з періодичною таблицею в руці.
Кроки
Метод 1 із 2: Знаходження кількості нейтралів у загальному атомі
Знайдіть елемент у періодичній таблиці. Для цього прикладу розглянемо ОС (Os), що знаходиться в шостому ряду, зверху вниз.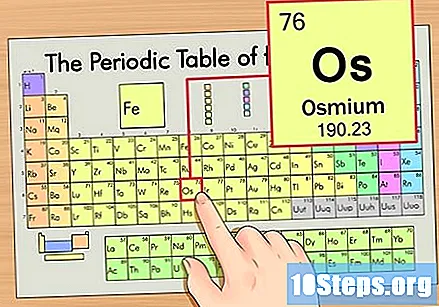
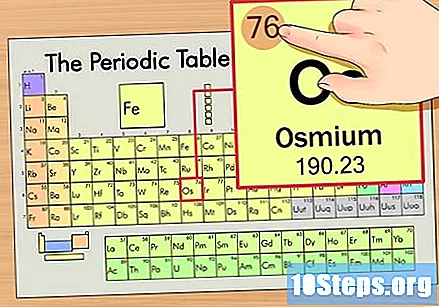
Знайдіть атомний номер елемента. Зазвичай це найбільш видиме число для певного елемента і, як правило, вище його символу (у таблиці, яку ми використовуємо, насправді іншого номера не вказано). Атомне число - це кількість протонів в одному атомі цього елемента. Кількість Os дорівнює 76, це означає, що атом Осмію має 76 протонів.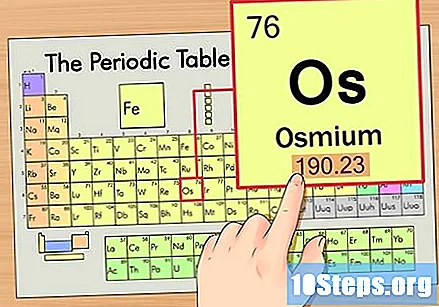
Знайдіть атомну масу елемента. Це число зазвичай знаходиться нижче атомного символу. Зауважимо, що таблиця в цьому прикладі заснована лише на атомному номері і не перераховує атомну масу. Це не завжди буде так. Асмій має атомну масу 190,23.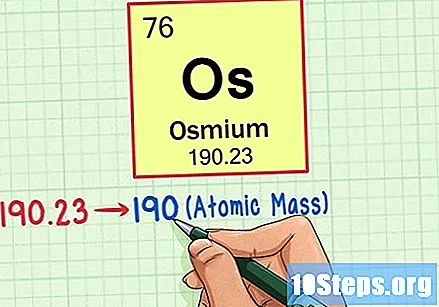
Округлете атомну масу до найближчого цілого числа, щоб знайти атомну масу. У нашому прикладі 190,23 було б округлено до 190, що призведе до атомної маси 190 для Осмія.- Атомна маса - це середнє значення ізотопів елемента. Тому зазвичай це не ціле число.
Відняти атомне число від атомної маси. Оскільки переважна більшість маси атома знаходиться в його протонах і нейтралах, віднімання кількості протонів (тобто атомного числа) від атомної маси дасть вам число розраховано нейтронів в атомі. Число після десяткової крапки зазвичай представляє дуже малу масу електронів в атомі. У нашому прикладі це: 190 (атомна маса) - 76 (кількість протонів) = 114 (кількість нейтронів).
Запам’ятайте формулу. Щоб знайти кількість нейтронів у майбутньому, просто використовуйте цю формулу: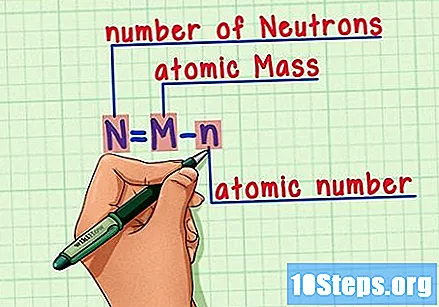
- N = M - n.
- N = кількість Nевтрони.
- М = Матомна смажена.
- n = натомна плечова кістка.
- N = M - n.
Метод 2 з 2: Знаходження кількості нейтронів в ізотопі
Знайдіть елемент у періодичній таблиці. Наприклад, давайте використовувати ізотоп вуглецю-14. Оскільки неізотопна форма вуглецю-14 є просто вуглецем (С), знайдіть цей елемент у періодичній таблиці (у другому ряду).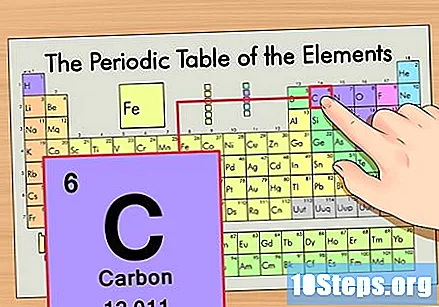
Знайдіть атомний номер елемента. Зазвичай це найбільш видиме число для певного елемента і, як правило, вище його символу (у таблиці, яку ми використовуємо, насправді іншого номера не вказано). Атомне число - це кількість протонів в одному атомі цього елемента. C - це число 6, що означає, що атом вуглецю має 6 протонів.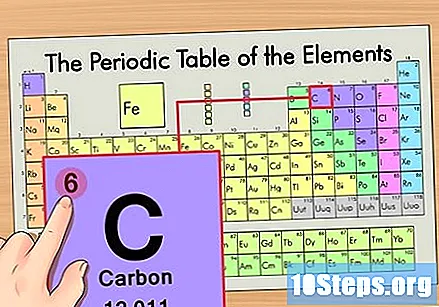
Знайдіть атомну масу. Це надзвичайно просто за допомогою ізотопів, оскільки вони названі за їх атомною масою. Вуглець-14 має атомну масу 14. Після того як ви знайдете атомну масу ізотопу, процес знаходження кількості нейтронів такий же, як у звичайних атомів.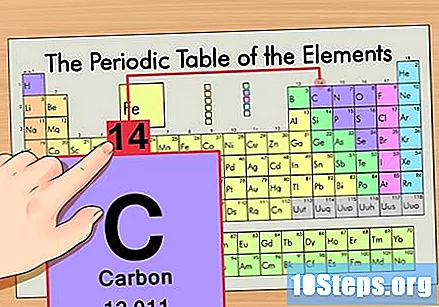
Відняти атомне число від атомної маси. Оскільки переважна більшість маси атома знаходиться в його протонах і нейтралах, віднімання кількості протонів (тобто атомного числа) від атомної маси дасть вам число розраховано нейтронів в атомі. Число після десяткової крапки зазвичай представляє дуже малу масу електронів в атомі. У нашому прикладі це: 14 (атомна маса) - 6 (кількість протонів) = 8 (кількість нейтронів).
Запам’ятайте формулу. Щоб знайти кількість нейтронів у майбутньому, просто використовуйте цю формулу: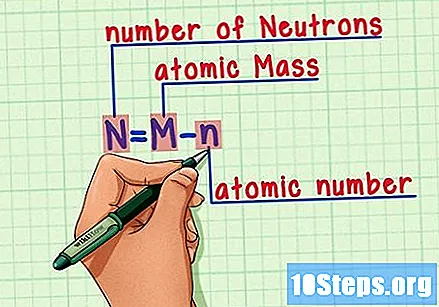
- N = M - n.
- N = кількість Nевтрони.
- М = Матомна смажена.
- n = натомна плечова кістка.
- N = M - n.
Поради
- Осьмій, твердий метал при кімнатній температурі, отримав свою назву від грецького слова «запах», «осма».
- Протони та нейтрони становлять майже всю масу елементів, тоді як електрони та інші різноманітні частинки представляють незначну масу (наближається до нульової маси). Оскільки протон має приблизно таку саму вагу, як нейтральний, а атомне число являє собою кількість протонів, ми можемо просто відняти кількість протонів від загальної маси.
- Якщо ви не впевнені, яке число є в періодичній таблиці, просто пам’ятайте, що воно зазвичай робиться навколо атомного числа (тобто кількості протонів), яке починається з 1 (Водень) і збільшується на одну одиницю на зліва направо, закінчуючи 118 (Ununóctio). Це тому, що кількість протонів в атомі визначає, що це за атом, полегшуючи впорядкування елементарної характеристики (наприклад, атом з 2 протонами завжди буде гелієм, подібно до того, що інший атом із 79 протонами завжди буде Золотом).


