Зміст
- етапи
- Спосіб 1 Збалансування рівняння методом проб і помилок
- Спосіб 2 Вирівняйте рівняння алгебраїчним методом
У хімії рівняння встановлює те, що сталося під час хімічної реакції. Зліва від рівняння розміщуємо реагенти, які були використані для експерименту, а праворуч - продукти, отримані в ході експерименту. За принципом збереження маси (Лавуазьє) під час хімічної реакції жоден атом не зникає, жоден не створюється, вони поєднуються по-різному. Підсумовуючи, ви повинні мати ту саму кількість дат кожного елемента праворуч, що і зліва від рівняння. Ось чому рівняння балансу завжди має бути збалансованим.
етапи
Спосіб 1 Збалансування рівняння методом проб і помилок
-
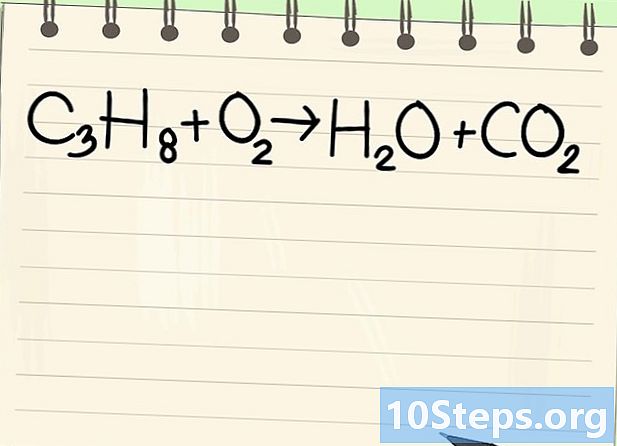
Зверніть увагу на рівняння балансу. Ми розглянемо таке рівняння:- З3H8 + О2 -> Н2O + CO2
- Це рівняння спалювання пропану (С3H8) у кисні: отримують воду та вуглекислий газ.
-
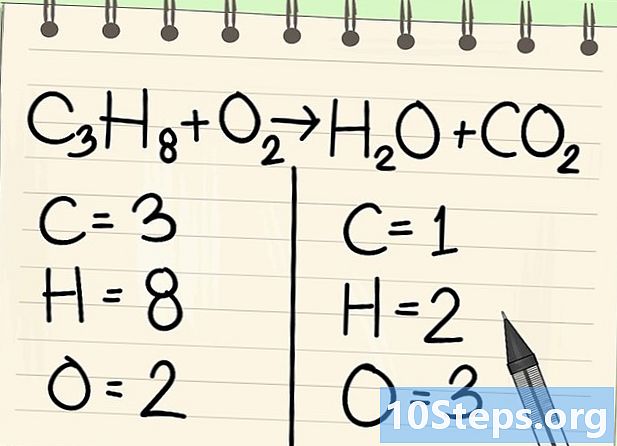
Порахуйте атоми. Введіть кількість дат кожного елемента з одного боку рівняння, а потім з іншого. Для цього враховуйте індекси, якщо таких немає, індекс дорівнює 1.- Зліва - 3 атоми вуглецю, 8 водню та 2 кисню.
- Праворуч - 1 атом вуглецю, 2 водню і 3 кисню.
-
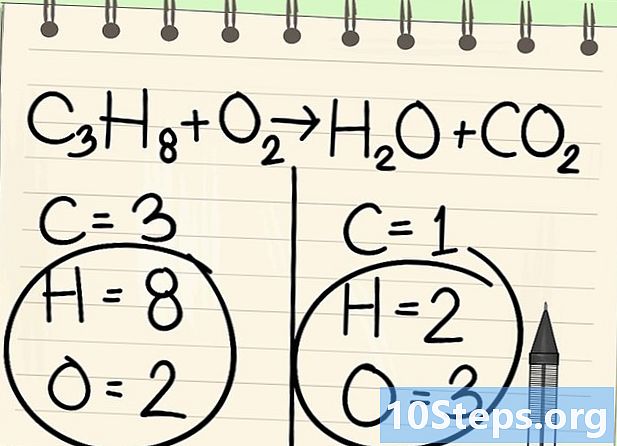
На мить залиште осторонь водень та кисень. -

Почніть балансувати з правим елементом. Ми завжди починаємо з того, хто знаходиться в молекулі до і після реакції. Якщо їх декілька, візьміть ту, яка одновалентна в одній з молекул. Тут ми починаємо з атомів вуглецю. -

Збалансуйте атоми вуглецю. Додайте праворуч коефіцієнт до молекули вуглекислого газу (СО)2), в якому вуглецевий латом один. Ми поставимо 3, щоб отримати 3 ліві атоми.- З3H8 + О2 -> Н2O + 3Колорадо2
- Таким чином, у нас справа 3 атоми вуглецю завдяки коефіцієнту (3CO)2) та 3 атоми вуглецю зліва завдяки індексу (C3H8).
- У рівняння ви можете покласти всі необхідні вам коефіцієнти, але дотиків не можна торкатися.
-
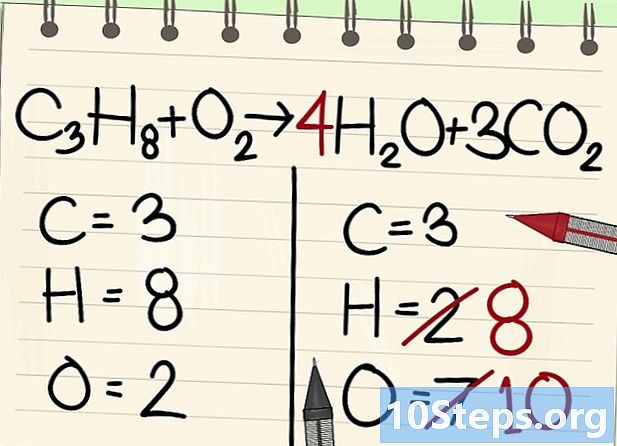
Збалансуйте атоми водню. Оскільки у вас є 8 зліва від рівняння, вам потрібно стільки ж праворуч.- З3H8 + О2 --> 4H2O + 3CO2
- Праворуч ви поставите коефіцієнт 4, оскільки водень є двовалентним у молекулі води: індекс 2 означає, що два атоми водню пов'язані.
- Щоб отримати кількість атомів водню праворуч, ви помножите коефіцієнт 4 на індекс 2, або 8 атомів.
- Що стосується атомів кисню, то праворуч їх 6 на одній стороні, що надходять від трьох молекул 3CO2 (3 х 2 = 6 атомів) і 4 з 4 молекул 4 Н2O (4 х 1 = 4 атоми), тобто загалом 10 атомів кисню.
-
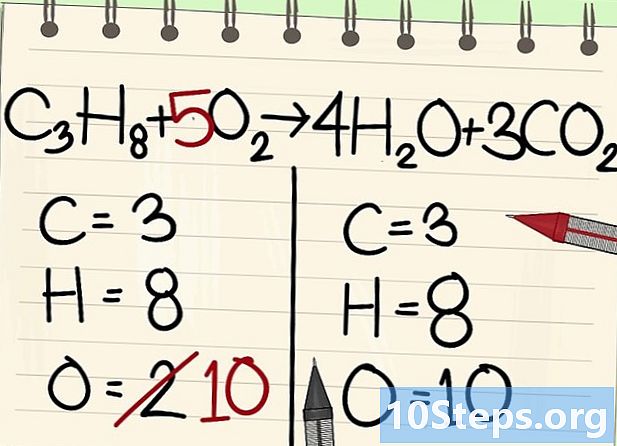
Збалансуйте атоми кисню.- Через баланс вуглецю та водню кількість атомів кисню не однакове з обох сторін рівняння. Раніше ми бачили, що праворуч знаходиться 10 атомів кисню (4 - від молекул води та 6 - від молекул вуглекислого газу). Зліва - лише 2 (від О2).
- Щоб збалансувати кисень, додайте коефіцієнт 5 до лівої молекули кисню: у вас 10 атомів кисню зліва, а другий праворуч.
- З3H8 + 5Про2 -> 4Н2O + 3CO2
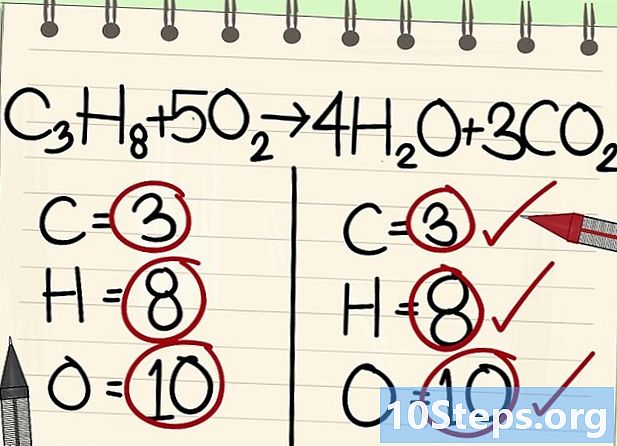
- Всі атоми (вуглець, водень та кисень) збалансовані: ваше рівняння збалансовано.
Спосіб 2 Вирівняйте рівняння алгебраїчним методом
-

Напишіть рівняння для балансування. Призначте кожній молекулі буквальний коефіцієнт. Ми їх назвемо має, б, з і d. -
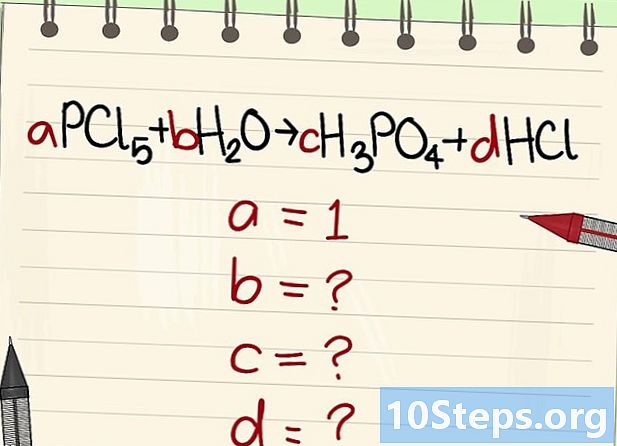
Знайдіть значення інших прямолінійних коефіцієнтів. Ми це запитаємо має = 1. -

Знайдіть зв’язки між цими коефіцієнтами. Поглянувши ліворуч (реагенти) та праворуч (продукти), встановіть зв’язки між цими різними коефіцієнтами.- Візьміть таке рівняння: aPCl5 + bH2O = cH3PO4 + dHCl. Було заявлено, що a = 1, що означає, що c = a, d = 5a та 2b = 3c + d. Проведені розрахунки, c = 1, d = 5 і b = 4.

- Візьміть таке рівняння: aPCl5 + bH2O = cH3PO4 + dHCl. Було заявлено, що a = 1, що означає, що c = a, d = 5a та 2b = 3c + d. Проведені розрахунки, c = 1, d = 5 і b = 4.