
Зміст
Атомний номер відповідає кількості протонів в ядрі окремого атома елемента. Це значення не змінюється; отже, ви можете використовувати його для виявлення інших характеристик ізотопу, таких як кількість нейтронів.
Кроки
Частина 1 з 2: Пошук атомного числа
Знайдіть копію таблиці Менделєєва. Натисніть тут, якщо у вас його немає. Кожен елемент має свій атомний номер; таким чином, немає ярликів для вивчення змісту. Скористайтеся копією таблиці або спробуйте запам’ятати її.
- У більшості книг з хімії стіл надрукований на задній обкладинці.

Знайдіть у таблиці елемент, який вивчаєте. Більшість таблиць містять повну назву елементів, а також їх символи (Hg для ртуті, наприклад). Якщо ви не можете знайти те, що шукаєте, підключіться до Інтернету та виконайте пошук за термінами «хімічний символ» та назвою елемента.
Знайдіть атомний номер елемента. Зазвичай він знаходиться у верхньому лівому або правому куті будинку елемента, але він може бути і в інших місцях. Крім того, це завжди ціле значення.- Якщо число включає десяткову крапку, це, ймовірно, вказує на атомну масу.
Підтвердьте інформацію відповідно до елементів поблизу. Періодична система організована відповідно до порядку атомних чисел. Наприклад, якщо ваше ізотопне число "33", елементом ліворуч буде "32", а праворуч - "34". У такому випадку це тому, що ви дивитесь на атомний номер.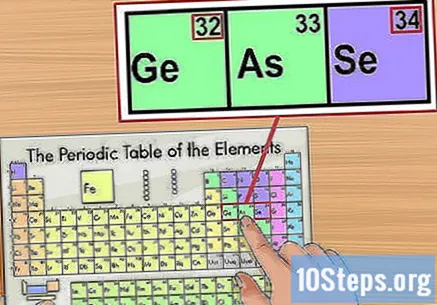
- Відбувається стрибок між елементами "56" (барій) і "88" (радіо). Ізотопи, які відповідають цьому діапазону, знаходяться у двох рядках нижче таблиці. Їх поділяють лише так, щоб стіл не був занадто великим.
Зрозумійте, що означає атомний номер. Атомний номер має просте визначення: кількість протонів в атомі елемента. Ця кількість протонів, у свою чергу, визначає загальний електричний заряд ядра - що, отже, визначає, скільки електронів може зарядити атом. Оскільки електрони відповідають за майже всі хімічні взаємодії, атомний номер побічно впливає на фізичні та хімічні властивості елемента.- Іншими словами, кожному атому з вісьмома протонами відповідає атом кисню. Два атоми кисню можуть мати різну кількість нейтронів, (якщо один є іоном) або електронів, але вони завжди матимуть по вісім протонів.
Частина 2 з 2: Виявлення більш важливої інформації
Визначте атомну вагу. Зазвичай він під назвою елемента в періодичній системі має два-три знаки після коми. Атомна вага відповідає середній масі атомів елемента, представляючи, як він знаходиться в природі. Він вимірюється в "одиницях атомної маси" ("u" або "u.m.a").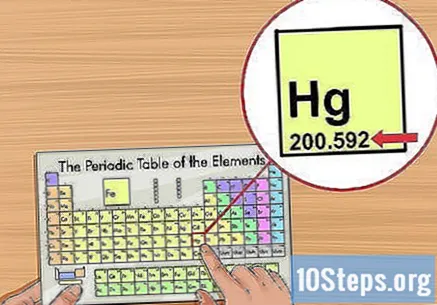
- Багато вчених вважають за краще використовувати термін "атомна маса" замість ваги.
Зрозумійте атомну масу. Поняття атомної маси дуже схоже на поняття ваги. Різниця полягає в тому, що вага вказує на середню масу будь-якого атома в елементі, а не конкретного атома. Наприклад: грам заліза містить кілька атомів з різною масою; вага вказує на їх "відносну масу". Якщо ви вивчаєте один атом елемента, вам просто потрібно знати його питому масу.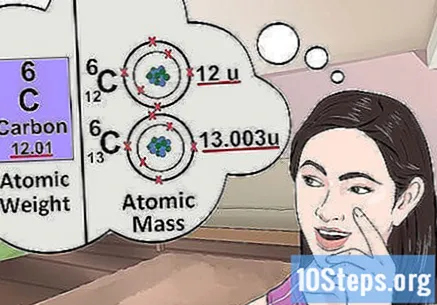
- Як правило, проблеми хімії, що стосуються лише атомів, вже повідомляють атомне масове число. Потрібно лише зрозуміти концепцію, щоб не застати вас зненацька, коли ви бачите інше значення.
Округліть масове число. Масове число відповідає загальній кількості протонів і нейтронів в атомі елемента. Розрахувати це не складно: просто візьміть атомну масу, надруковану на періодичній таблиці, і округніть її до найближчого цілого значення.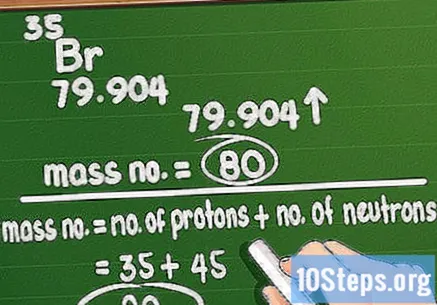
- Це працює, оскільки кількість нейтронів і протонів дуже близька до 1 м.д.м., тоді як кількість електронів дуже близька до нуля. Атомна маса передбачає точні розрахунки для визначення десяткового значення, але єдиними даними, які мають значення, є цілі числа, які вказують вам, скільки протонів і нейтронів.
- Пам'ятайте, що якщо ви використовуєте атомну масу, ви зіпсуєте вагу конкретного атома в елементі. Наприклад, зразок брому має атомну масу 79 або 81.
Обчисліть кількість нейтронів. Тепер ви вже знаєте, що атомний номер дорівнює кількості протонів і що масове число дорівнює сумі числа протонів і нейтронів. Щоб визначити кількість нейтронів в елементі, просто відніміть атомне число від цієї загальної маси. Кілька прикладів:
- Атом гелію (He) має масове число 4 і атомний номер 2. Отже, 4 - 2 = 2 нейтрони.
- Зразок срібла (Ag) має середнє масове число 108 (згідно з періодичною системою) і атомний номер 47. В середньому кожен атом у зразку має 108 - 47 = 61 нейтрон.
Зрозумійте ізотопи. Ізотоп - це специфічна форма елемента, що містить певну кількість нейтронів. Якщо проблема, яку ви хочете вирішити, має щось на зразок "бор-10" або "В", це тому, що ви говорите про елементи бору з масовим числом 10. Використовуйте це значення, а не "нормальні" значення бору.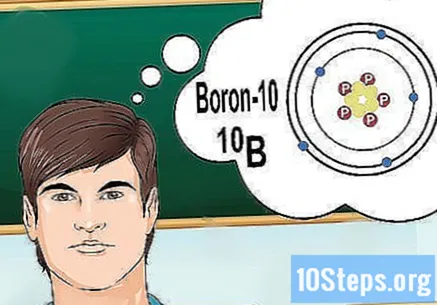
- Атомний номер ізотопів ніколи не змінюється. Кожен ізотоп елемента має однакову кількість протонів.
Поради
- Атомна вага деяких важчих елементів подається в дужках або квадратних дужках. Це означає, що ця вага є точною масою найбільш стабільного ізотопу, а не в середньому кількох ізотопів. Нарешті, це не впливає на атомний номер елемента.


