
Зміст
Інші розділиВодень є найлегшим елементом і має багато промислових цілей, включаючи створення гідрованих жирів для використання на кухні та виробництво вуглеводнів із вугілля. Він є важливою частиною молекул води і може бути відокремлений за допомогою невеликої кількості електроенергії. Ви також можете виробляти газоподібний водень, використовуючи деякі активні метали та сильні кислоти. Обидва методи відносно прості і дозволять збирати газоподібний водень.
Кроки
Метод 1 із 2: Використання водовідведення з активними металами
Зберіть необхідні матеріали. Для збору водню, використовуючи реакцію змішування сильної кислоти з активним металом, вам знадобляться: колба Ерленмейера, гумова пробка, пластикові трубки, дистильована вода, пробірки, великий контейнер, 3 молярна соляна кислота (HCl) і магнієві або цинкові гранули.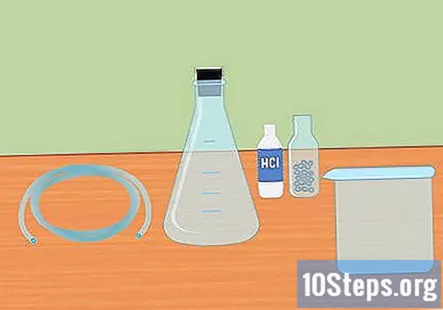
- Колба Ерленмейера - скляна колба, що має конічне дно і циліндричну горловину.
- Гумова пробка призначена для верхньої частини колби і повинна мати отвір посередині для проходження трубки.
- Для цього експерименту підійдуть або магній, або цинк, і те, і інше вам не потрібно.
- Деякі з цих витратних матеріалів, можливо, доведеться придбати в Інтернеті або в лабораторному магазині.

Носіть належні захисні засоби. Працюючи з сильною кислотою, такою як соляна кислота, ви хочете переконатися, що дотримуєтесь належних заходів безпеки. Надягати лабораторне пальто, рукавички, закрите взуття та захист очей дуже важливо.- Окуляри повинні обернути сторони очей, щоб захистити їх від бризок.
- Одягайте рукавички, які належним чином прилягають, щоб ви зберігали спритність рук і пальців.
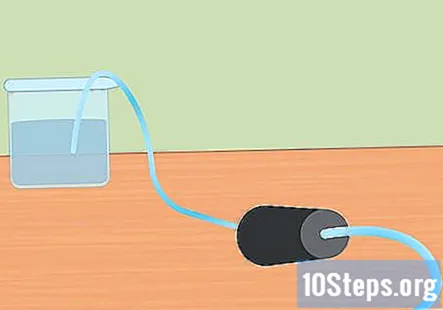
Підготуйте експериментальну установку. Вставте один кінець трубки в отвір гумової пробки. Ви хочете, щоб трубка пройшла весь шлях через гумову пробку і трохи стирчала з кінця. Наповніть велику ємність водою і помістіть вільний кінець трубки у воду. Коли експеримент розпочнеться, ви вставите гумову пробку в колбу Ерленмейера.- Відкладіть ці шматки в сторону, поки не будете готові їх використовувати.
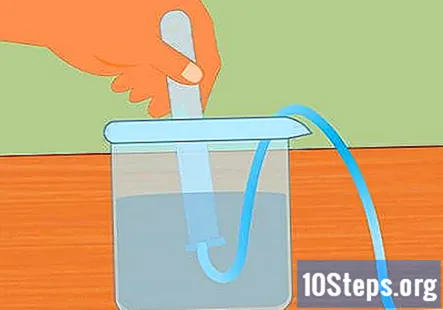
Занурте пробірку у воду. Візьміть принаймні одну пробірку (ви можете використовувати більше, якщо хочете зібрати більше водню) і занурте її у воду. Нахиліть трубку, щоб усі бульбашки повітря могли вийти. Покладіть трубку поверх зануреної трубки, прикріпленої до гумової пробки на протилежному кінці.- Дуже важливо, щоб усі бульбашки повітря були видалені з трубки перед початком роботи. Якщо їх немає, газ, зібраний у трубці, буде не просто воднем.
Додайте соляну кислоту в колбу Ерленмейера. Додайте стільки соляної кислоти, щоб наповнити колбу приблизно наполовину. Приблизно 100 мл має бути достатньо. Перед додаванням кислоти переконайтеся, що колба є чистою і сухою. Одягайте гумові рукавички та будьте обережні, наповнюючи колбу.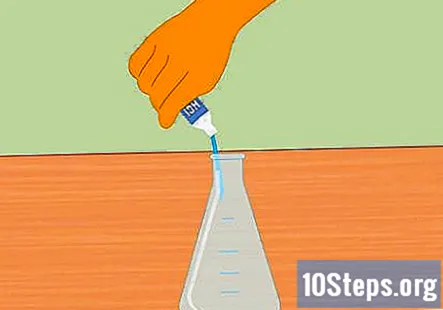
- Будьте обережні, щоб не розлити воду в кислоту. Додана в кислоту вода може призвести до вибуху та травмування.
Розпочніть хімічну реакцію додаванням металевих гранул до HCl. Додайте в соляну кислоту в колбі жменьку гранул цинку або магнію. Точна сума, яку ви вводите, не важлива, але для початку реакції має бути достатньо невеликої купки.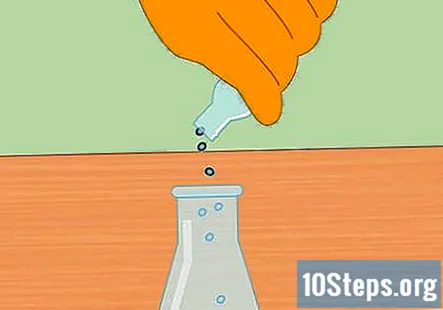
- Після додавання гранул помістіть пробку в колбу так, щоб система тепер була закрита.
Зберіть водень у занурену пробірку. Коли метал реагує з кислотою, утворюється газоподібний водень. Цей водень рухається до верхньої частини колби, через трубку і в пробірку, занурену у воду. Газ витіснить воду, і ви повинні побачити міхур у формі у верхній частині пробірки.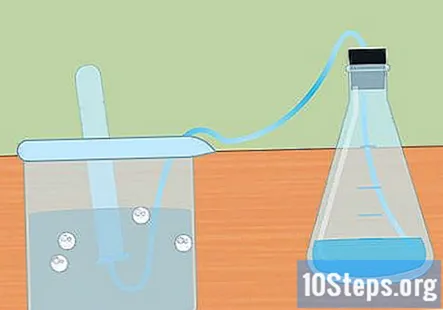
- Коли пробірка наповниться воднем, занурте іншу пробірку водою і поставте її над пробіркою. Ви можете зібрати стільки водню, скільки утворюється в результаті вашої реакції.
- Тримайте пробірки донизу, щоб запобігти виходу газоподібного водню в повітря.
Переконайтеся, що газ - водень. Для того, щоб підтвердити, що газ є воднем, ви можете зробити те, що називається тест на шину. Запаліть сірник і потримайте його під трубкою. Ви почуєте звук "поп" або писк, який вказує на наявність водню.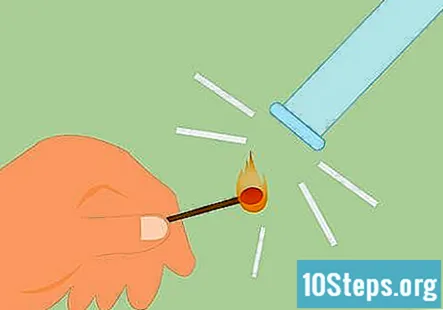
Метод 2 з 2: Використання електролізу
Зберіть необхідні матеріали. У цьому експерименті ви будете використовувати електрику, щоб відокремити газ водню та кисню від молекул води. Для збору газоподібного водню за допомогою електролізу вам знадобиться 9-вольтовий акумулятор, олівець, дві пробірки, пластиковий контейнер, вода, харчова сода, дві великі гумки (за бажанням) та затиск для акумулятора з фіксаторами на кінці.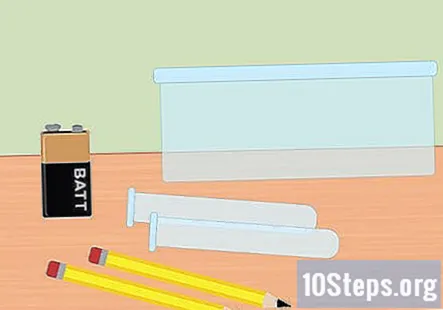
- Щоб це працювало, олівець повинен мати графіт. Олівець номер 2 ідеально підходить. Два невеликі шматочки графіту також підійдуть для цього.
- Достатньо невеликого контейнера або миски для зберігання продуктів.
- Переконайтесь, що затискач для акумулятора вміщує 9-вольтовий акумулятор, і що на ньому є червоно-чорний провід із затискачами-крокодилами на кінці. Ці затискачі будуть використовуватися для підключення вашої системи до акумулятора.
Зніміть гумку з олівця і розламайте олівець навпіл. Вам потрібні два шматочки графіту, один для позитивного кінця акумулятора і для негативного кінця акумулятора. Заточіть обидва кінці кожного шматка олівця до точки. Переконайтесь, що графіт добре видно.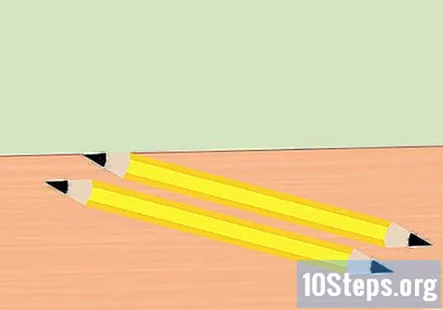
- Цей крок можна пропустити, якщо у вас вже є два шматки чистого графіту.
Оберніть навколо контейнера 2 гумки у формі Х. Цей крок є необов’язковим, але це простий спосіб утримувати пробірки на місці під час проведення експерименту. Протягніть одну гумку над контейнером і протягніть над нею другу гумку, щоб вона перетиналася над першою, утворюючи X.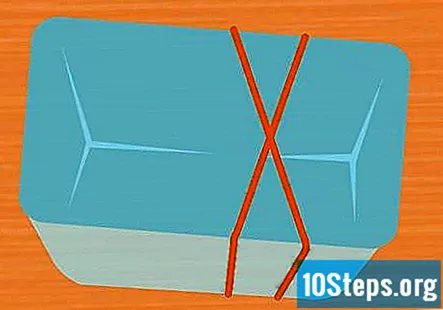
- Якщо ви не використовуєте гумки, обов’язково закріпіть пробірки скотчем або ниткою, щоб вони залишалися догори дном під час експерименту.
Зробіть розчин харчової соди та води. Розчинення харчової соди у воді допоможе проводити електроенергію в системі. Точна кількість доданої харчової соди не є важливим, але приблизно 1 чайної ложки на 1 склянку води має бути достатньо. Перемішувати до повного розчинення.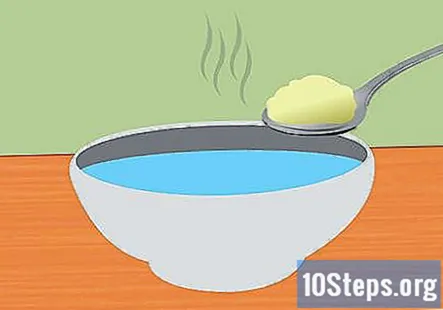
- Використовуйте теплу воду, щоб прискорити розчинення харчової соди.
Наповніть пластиковий контейнер і пробірки розчином харчової соди. Ємність повинна бути достатньо великою, щоб вмістити обидві пробірки. Додайте достатньо розчину, щоб заповнити ємність приблизно на три чверті. Занурте пробірки в розчин контейнера і переверніть їх догори дном. Помістіть кожну трубку в хрест гумки X, щоб утримувати її на місці.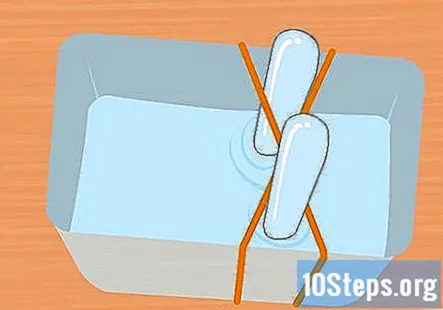
- Дуже важливо, щоб обидві пробірки були повністю заповнені водою і не залишалося бульбашок повітря.
Прикріпіть затискачі алігатора до графіту. Візьміть один затискач із затиску акумулятора і прикріпіть його до кінця одного з олівців. Переконайтеся, що він торкається якомога більшої частини графіту. Зробіть те ж саме з рештою затискачем алігатора та олівцем.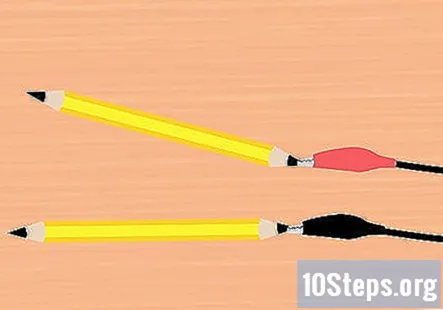
- Один олівець слід прикріпити до червоного затискача, а один олівець до чорного затиску.
Вставте незатиснутий кінець олівця у пробірку. Тримаючи пробірку повністю зануреною, злегка нахиліть її, щоб ви могли просунути незатиснутий кінець олівця в пробірку. Повторіть цей процес з іншим олівцем та іншою пробіркою.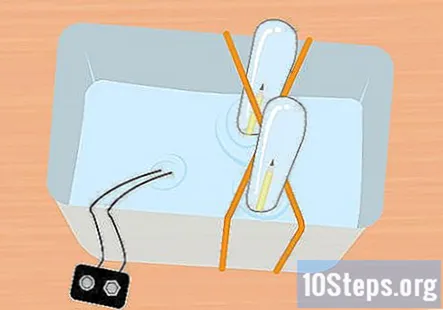
- На цей момент все повинно бути під водою, а всередині кожної пробірки повинен бути один шматок олівця.
- Тримайте кінець затиску для акумулятора, який кріпиться до акумулятора, поза водою.
Прикріпіть затискач акумулятора до 9-вольтової батареї. Після того, як все налаштовано, ви тепер готові подавати електроенергію, що забезпечується 9-вольтовим акумулятором. Кінець затискача батареї повинен стирчати з контейнера, тому просто закріпіть акумулятор на місці. Як тільки батарея буде приєднана, ви повинні помітити, що бульбашки піднімаються з кінця графіту і плавають у верхній частині кожної пробірки.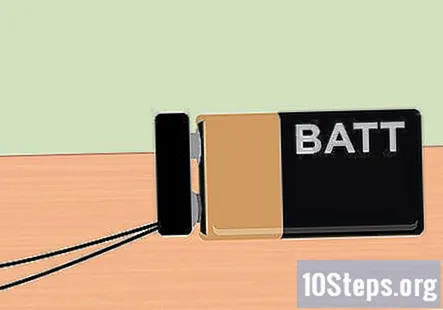
- Якщо ви не бачите бульбашок, переконайтесь, що затискачі алігатора надійно прикріплені до графіту олівця. Також перевірте, чи повністю заряджений ваш акумулятор.
- Пробірка з негативним проводом, прикріпленим до олівця, буде виробляти водень, тоді як пробірка, прикріплена до позитивного дроту батареї, буде виробляти кисень.
Збирайте водень і кисень у двох пробірках, поки у вас не буде декількох дюймів газу в кожній пробірці. Пам’ятайте, у трубці, під’єднаній до мінусового кінця батареї, буде водень, а кисень буде в трубці, під’єднаній до позитивного кінця. Вийміть пробірки з банки по черзі. Тримайте їх догори дном і дайте воді стекти. Газ у пробірках залишатиметься, хоча ви його не бачите.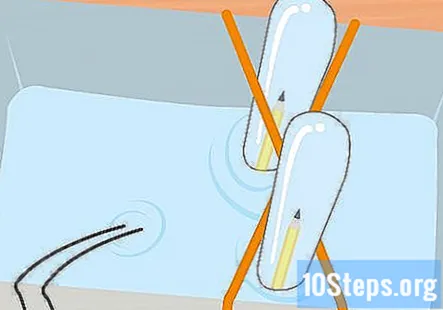
Тест на наявність водню. Ви можете перевірити наявність водню, вдаривши сірник і піднявши полум’я до газу. Це буде видавати дуже чіткий "скрипучий поп", якщо це водень. Ви також можете використовувати запалену свічку замість сірника.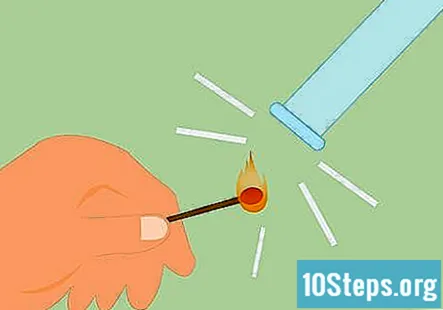
- Щоб перевірити наявність кисню в пробірці, яка була підключена до позитивної сторони джерела живлення, задуйте запалену сірник (або свічку) і поставте все ще світиться кінець під пробірку. Якщо свічка відновлюється, присутній кисень.
Питання та відповіді спільноти
Чи потрібні дві пробірки, якщо я хочу збирати лише водень?

Науковець з навколишнього середовища Бесс Рафф - докторант географії в Університеті штату Флорида. Вона здобула ступінь магістра екологічних наук та менеджменту в Університеті Каліфорнії в Санта-Барбарі в 2016 році. Вона провела обстеження проектів морського просторового планування в Карибському басейні та надала наукову підтримку в якості випускника Групи сталого рибальства.

Скільки водню можна зібрати з цього простого експерименту електролізу? І яким би був тиск газоподібного водню?
Це залежить. Швидкість реакції (розщеплення води) базується на підсилювачах батареї та часу, що залишився на реакцію. Зазвичай водень мав би тиск приблизно на рівні моря, якщо ви не будете проводити експеримент у справді гарячому або холодному середовищі.
Чому водень збирається в мінусовій трубці
Завдяки тому, як молекули води діляться електронами, атоми Гідрогену заряджені позитивно, а атоми Оксигену - негативно. При витяганні газів позитивно заряджений водень буде притягуватися до негативної трубки, тоді як негативно заряджений кисень - до позитивної трубки.
Чому газ не витікав із моєї трубки для збору газу?
Це водень, газ, який легший за всі інші, включаючи гелій, що означає, що він буде залишатися в пробірці до тих пір, поки закритий кінець пробірки знаходиться зверху, оскільки інші гази витісняють його. Причиною того, що ми використовуємо гелій замість водню, є те, що він не є займистим. Це пов’язано з тим, що це благородний газ (він має повну валентну оболонку з 8 електронів) і тому не реагує.
Газ був би дуже займистим?
Так. Дивіться катастрофу в Гінденбурзі на YouTube. Цепеліни використовували водень, оскільки він був найлегшим газом, і його досить легко отримати. Ось чому деякі виробники автомобілів працюють на автомобілях з водневим двигуном.
це рідка форма водню?
Ні - водень у цьому експерименті буде газоподібним
Як зріджувати водень? Відповідь
Попередження
- Будьте обережні з чистим воднем. Він дуже вибухонебезпечний при змішуванні з повітрям.
- Переконайтеся, що все інше повітря було видалено з обладнання, в якому ви збираєте водень.


